子宮頸がんについて
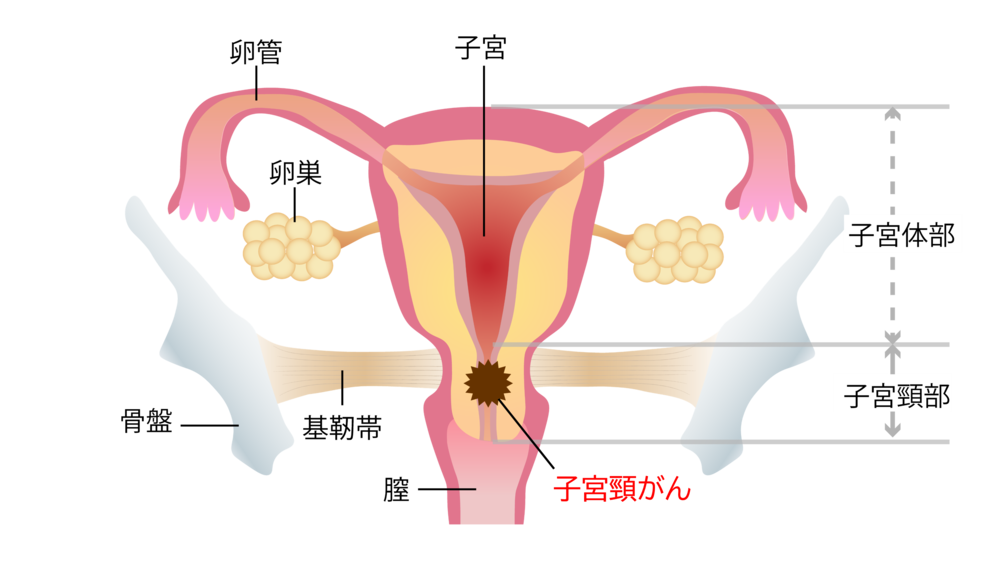
子宮がんには、子宮の入り口(子宮頸部)にできる「子宮頸がん」と、子宮の奥の袋状の部分(子宮体部)にできる「子宮体がん」の2種類があります。このうち「子宮頸がん」は、子宮がん全体の約3割を占めています。
以前は40~50代の女性に多く見られましたが、最近では30~40代が中心となり、若年化が進んでいます。20代で発症するケースも増えており、妊娠・出産を望まれる世代にとって重大な影響を及ぼすがんです。
日本では毎年約1万人の女性が子宮頸がんにかかり、約3,000人が亡くなっています。
子宮頸がんの原因:HPV感染
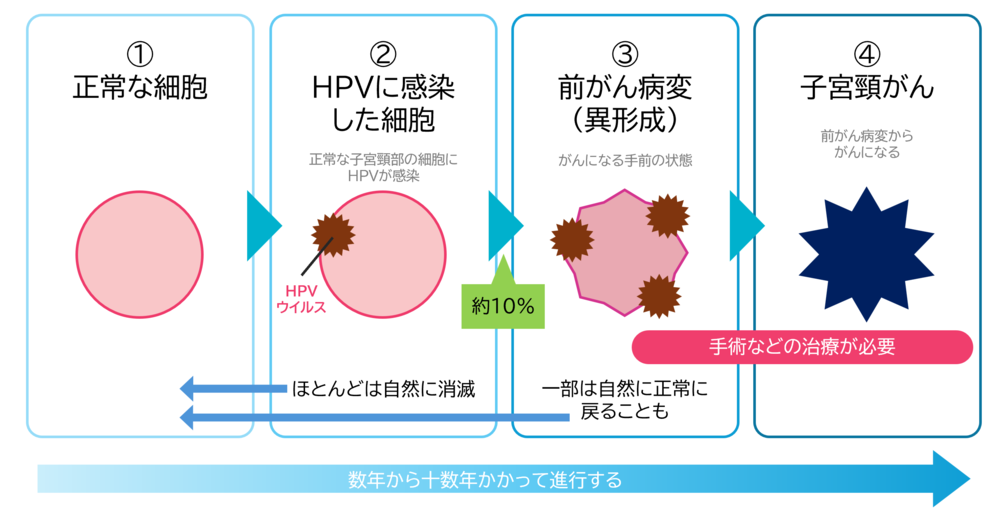
子宮頸がんのほとんどは、ヒトパピローマウイルス(HPV)の感染が原因であることが分かっています。HPVは性的な接触によって男女ともに感染するありふれたウイルスで、性交経験のある女性の約80%が生涯に一度は感染するといわれています。
多くの場合、感染しても免疫によって自然にウイルスは消えますが、約10%の女性ではHPVが体内に残り続けてしまいます。その一部の方が、がんの前段階である「異形成(子宮頸部上皮内病変:CIN)」という状態を経て、子宮頸がんを発症することがあります。
がんになる前に見つけるために
異形成の状態は数年続くことが多く、その間は不正出血や痛みなどの自覚症状がほとんどありません。だからこそ、子宮頸がん検診がとても重要です。
検診によって異形成を早期に発見できれば、「子宮頸部円錐切除術」という子宮を残す手術で治療することが可能です。これは、進行がんになる前に治療できる大きなメリットです。
HPVワクチンによる予防
最近では、HPVワクチンによって感染を予防できることがわかっています。性交渉を始める前にワクチンを接種することで、HPVの感染や異形成、子宮頸がんのリスクを大きく減らすことができます。
また、喫煙も子宮頸がんのリスクを高めることが知られており、タバコを吸う方はより注意が必要です。
子宮頸がんの組織型と傾向
日本における子宮頸がんの組織型には、以下の2つがあります。
| 扁平上皮がん | 子宮の入り口の表面にある「扁平上皮細胞」からできるがんです。子宮頸がんの約75%を占め、腺がんに比べて放射線が効きやすいです。 |
|---|---|
| 腺がん | 子宮の奥に近い部分の「腺細胞(円柱上皮細胞)」からできるがんです。子宮頸がんの約23%を占め、近年では腺がんの割合が増加傾向にあります。 |
子宮頸がんの症状
子宮頸がんの初期や、がんになる前の「異形成」という状態では、ほとんどの場合、自覚症状がありません。
そのため、こうした無症状の方の多くは、子宮がん検診で見つかっています。
子宮頸がんの自覚症状としては、次のようなものがあります。
- 月経以外の出血(不正出血)
- 水っぽい・においが強いなど、おりものの異常
- 性交時の出血(接触出血)
がんが進行すると、下腹部痛や腰痛(腎臓に負担がかかることで起こる「水腎症」と呼ばれる状態)が起こることがあります。
また、膀胱や直腸にまで広がってくると尿や便に血が混じるといった症状がみられることもあります。
子宮頸がんの診断方法(検査方法)
子宮頸がんを調べるための検査には、以下のような方法があります。
| 細胞診 | 子宮の入り口を器具でこすって細胞を採取する方法 |
|---|---|
| 組織診(生検) | 子宮の入り口の組織を一部取り、顕微鏡で詳しく調べる方法 |
細胞診の結果はすべて”疑い診断”のため、がんが目で見てはっきりしないときには、コルポスコープという拡大鏡を使って子宮頸部を詳しく観察し、異形成やがんを疑う部分を狙って生検を行います。これを「コルポスコープ下生検」や「狙い撃ち生検」による組織診と言います。
また、細胞診ではがんの疑いがあるのに、コルポスコープや生検で異常が見つからない場合には、診断のために「子宮頸部円錐切除術」という手術を行うこともあります。
がんの進行度(ステージ)を決めるための検査
がんの広がり具合(進行期)によって治療方法が変わってくるため、治療開始前にさまざまな検査を行って進行期を決定します。手術を行った場合には、切除した臓器や組織の病理診断によって最終的な進行期が決まります。
進行期を決めるための検査には以下の方法があります。
| 婦人科的診察 | 内診・超音波検査などの基本的な診察で、がんの広がりを確認します。 |
|---|---|
| 画像検査 | CT・MRI・PETなどを用いて、がんの進行度や他臓器への影響を調べます。 |
| 内視鏡検査(必要時) | 泌尿器科・消化器内科に依頼し、膀胱や直腸への浸潤の有無を確認します。 |
 内診の様子 |
 MRI検査の様子 |
 内視鏡検査の様子 |
血液検査による補助的な診断
血液検査では「腫瘍マーカー」と呼ばれる、がんの種類によって血液中に現れる特有の物質を調べます。子宮頸がんの場合には、SCC・CEA・CA125・CA19-9などの腫瘍マーカーを測定します。
これらは、がんのタイプに応じて複数を組み合わせて測定します。ただし、この検査だけでがんがあるかどうかを確定することはできません。がんがあっても数値が上がらないことがあり、逆にがんがなくても、数値が高くなることもあります。そのため、腫瘍マーカーはあくまで補助的な検査方法して用いられます。
子宮頸がんの治療方法
治療方法は、各がん治療ガイドラインで推奨されている進行期に応じた治療方法、患者さんの年齢や持病などの体の状態、そして患者さんご自身の希望などをふまえて検討し、最終的に決定します。
子宮頸がんの治療には以下の方法があります。
- 手術療法
- 放射線治療
- 化学療法(抗がん剤治療)
これらを単独で行う場合と、いくつかを組み合わせる「集学的治療」を行う場合があります。
手術療法・機能温存治療について
子宮頸がんは、20~30代の女性に多く発症し、乳がんに次いで2番目に多いがんです。将来妊娠を希望される方も多いため、子宮を残す治療が重要です。
◆初期がんに対する温存手術
| 子宮頸部高度異形成・上皮内がん・初期の浸潤がん(ⅠA1期まで) | 子宮頸部円錐切除術で子宮を残したまま治療できる可能性があります。 |
|---|---|
| 腫瘍の大きさが2cm以下で子宮温存を希望する場合 | 広汎子宮頸部切除術(トラケレクトミー)という子宮頸部のみを摘出する手術も選択肢となります。 |
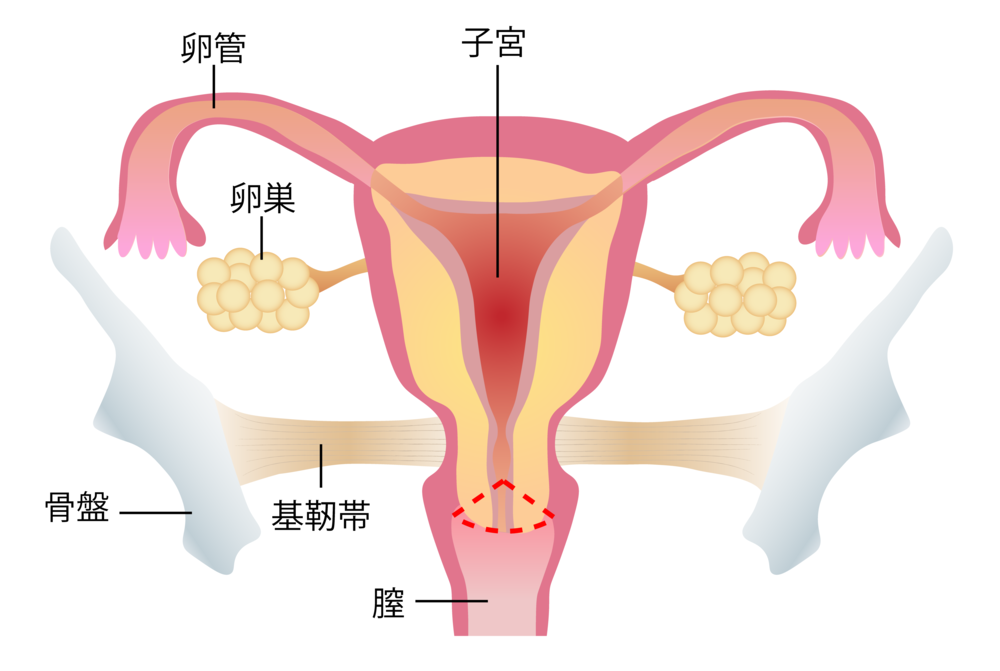 子宮頸部円錐切除術の切除範囲 |
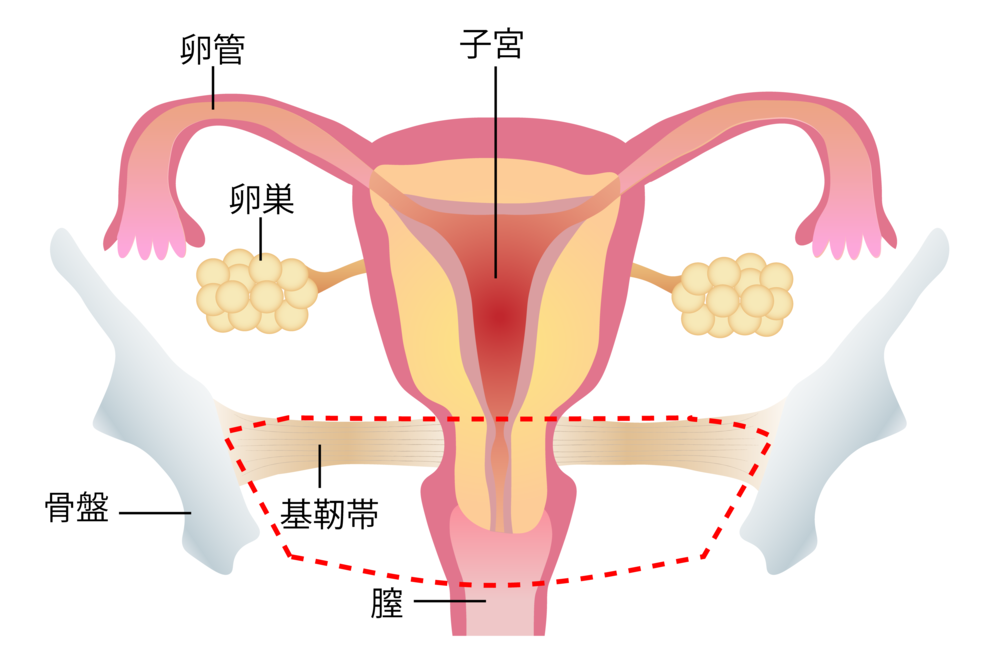 広汎子宮頸部切除術の切除範囲 |
◆子宮を残す希望がなく、がんが進行している場合
| ⅠA2~ⅡA期(場合によってはⅡB期) | 広汎子宮全摘術という、子宮とその周囲の組織を広く切除する手術を行います。 |
|---|
- 手術では、骨盤神経をできるだけ残す方法を取り入れ、排尿機能の温存を図ります。
- 年齢や病状によっては、卵巣を残すこともあります。
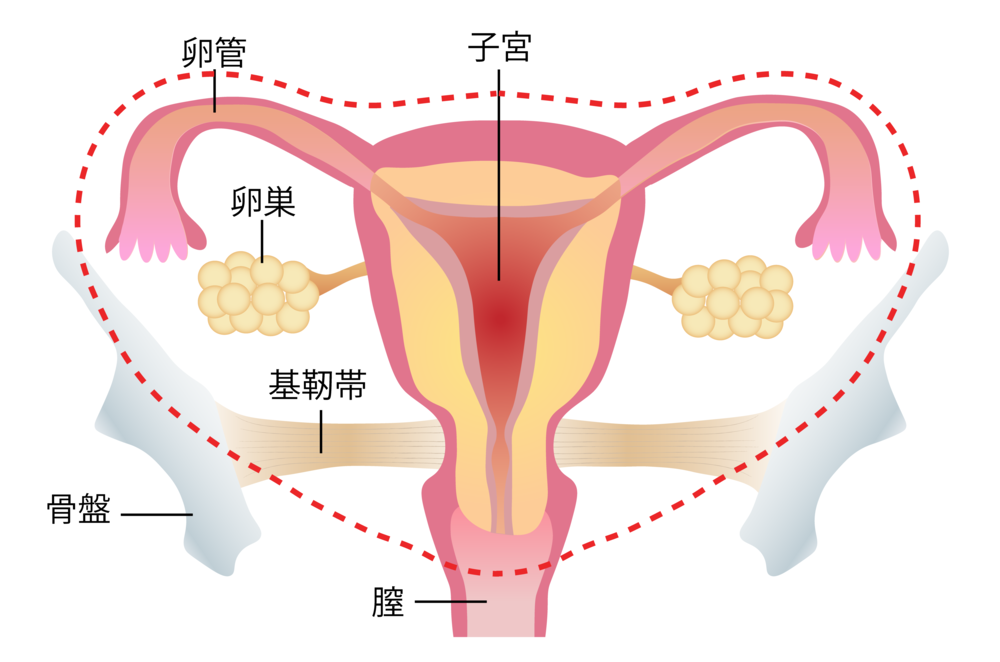 広汎子宮全摘術の切除範囲 |
放射線治療について
子宮頸がん(特に扁平上皮がん)は、放射線治療がよく効くことが知られています。
| ⅡB~ⅢB期(場合によってはⅣA期) | 腔内照射を併用した放射線治療が行われ、手術と同等の効果が期待されます。 |
|---|---|
| 高齢者や持病のある方 | Ⅰ期・Ⅱ期でも放射線治療が選択されることがあります。 |
放射線治療に抗がん剤を併用することで、より高い効果が期待できます。これを「同時化学放射線療法(CCRT)」といいます。
化学療法(抗がん剤治療)について
Ⅳ期の患者さんには、主に抗がん剤治療が行われます。
抗がん剤治療によってがんが小さくなった場合には、同時化学放射線療法(CCRT)に切り替えることもあります。
再発時には、状態に応じて手術・放射線・抗がん剤治療を単独または組み合わせて行います。
抗がん剤治療では、以下のような薬を単独または組み合わせて使用します。
| 白金製剤 | シスプラチン、カルボプラチン、ネダプラチン |
|---|---|
| その他の抗がん剤 | パクリタキセル、イリノテカン、ノギテカン |
| 分子標的薬 | ベバシズマブ |
| 免疫チェックポイント阻害薬 | ペンブロリズマブ・セミプリマブ |
| 抗体薬物複合体(ADC) | チソツマブベドチン |
当院の治療の特徴
腹腔鏡手術による低侵襲治療
当院は、子宮頸がんに対する腹腔鏡手術の施設基準を満たしており、腹腔鏡による手術が可能です。
腹腔鏡手術とは、お腹に小さな穴を開けてカメラや器具を挿入し、体内を映しながら行う手術で、開腹手術に比べて体への負担が少ないのが特徴です。
しかし、2018年に発表された海外の大規模研究(NEJM掲載)では、腹腔鏡手術は開腹手術よりも治療成績が劣るという報告がありました。その後の研究では、がんが小さい場合に慎重な手術操作を行えば、治療成績に差はないという報告も出ていますが、現時点では慎重な対応が求められています。
そのため、当院では以下のように対応しています。
- 子宮頸部円錐切除術で早期の浸潤がんと診断された患者さんに限り、腹腔鏡手術を導入
- 今後は、安全性と根治性を高めながら、適応範囲を徐々に拡大していく予定です
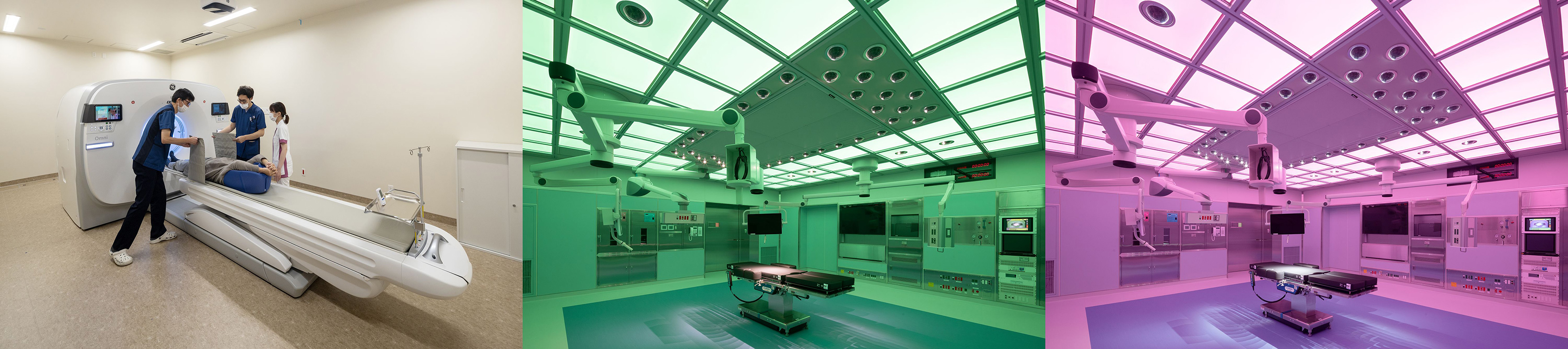
重粒子線治療による進行がんへの対応
当院では、大阪重粒子線センターと連携し、進行した子宮頸がんに対して重粒子線を用いた同時化学放射線治療を行っています。
重粒子線治療は、がん細胞を高精度で狙い撃ちし、正常組織への影響を抑えながら高い治療効果を発揮する先進的な放射線治療です。
この治療は、以下のような患者さんが対象です。
- 手術で完全にがんを取り除くことが難しい進行した子宮頸部腺がん
- 腫瘍の大きさが6cm以上の子宮頸部扁平上皮がん
これまでに、関西圏だけでなく、秋田県から沖縄県まで全国から患者さんを受け入れており、広域からの信頼を得ています。